新たな「ものさし」の開発を通じ、生命科学や医療に変革をもたらす!
Development of innovative analytical methods for life science and medical care
生命現象を詳細に理解するには「測る」という操作が必要不可欠です。何が、何処に、どれだけ、どのような状態で存在するかを調べることで、健康や病気に関する様々な情報が得られます。私達はユニークなアイデアと最先端の分析機器を駆使し、① これまで測れなかったものを測定可能にする、② これまで測れていたものをもっと高感度に、簡便に測定するための分析法開発を行っています。
我々の分析法は各種疾患の早期発見や再発予防、薬効評価、さらには新薬開発に繋がると考え、研究を行っています。
To understand the biological phenomena in detail, it is indispensable to “measure”. By investigating what, where, how much, and what state it exists, various information on health and illness can be obtained. By using unique ideas and state-of-art analytical instruments, we are developing new analytical methods (1) to make measurable what could not be measured so far, (2) to measure what have been measured more easily and conveniently. We believe that our analytical methods would contribute to early diagnosis of various diseases, relapse prevention, drug evaluation and drug development.
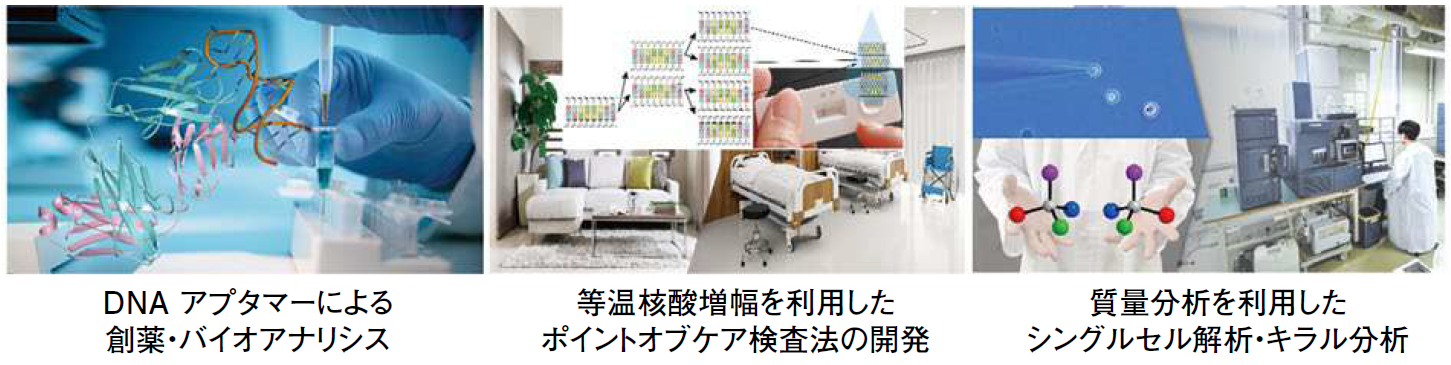
Research projects/研究内容
主な研究テーマ
(1) 超微量成分の高感度・高精度分析法の開発
(2) 次世代バイオ医薬品の新規分析法開発
(3) 迅速・簡便な核酸増幅診断法の開発
(4) 光学活性物質の高感度分離分析法開発
(5) 単一細胞メタボロミクスの開発
(6) メタボロミクス的アプローチによる新規バイオマーカー探索
(7) 高選択的分子イメージング法の開発
私達の第3研究室(轟木研究室)の研究テーマは,抗体医薬や次世代バイオ医薬のバイオ・プロセス・クリニカルアナリシス,診断や治療に利用するための新規DNAアプタマー開発,ポイントオブケア診断法の開発など多岐に亘っています。
血中に存在する抗体医薬を分析する場合,血中に多量に存在するIgGタンパク質の中から,相補性決定領域のみが異なる抗体医薬のみを選択的に認識しなければならない技術的困難さがあります。従来は抗抗体を用いて分子認識したり,トリプシン消化により生じた抗体医薬特異的なペプチド断片をLC-MS/MSで分析する手法が採られてきました。
私達は,抗体医薬bevacizumabを特異的に認識する世界初のDNAアプタマーを開発し,これを用いた実用的な分析法を報告しました(Anal. Chem., 91, 3125 (2019),Molecules, 24, 857 (2019),Chromatography, 43, 73 (2022),Anal. Sci., 39, 125 (2023))。アプタマーとは,複雑な三次元構造をとることで標的分子に結合する1本鎖の核酸分子であり,抗体に比べ安価で化学・物理的に安定,均質で配列さえわかれば世界中で容易に利用可能という利点があります。
また,これまで成功率が実施者の技量に大きく依存していたDNAアプタマー探索プロトコルを自動化,省力化するための手法を報告しました(J. Pharm. Biomed. Anal. Open, 1, 100006 (2023))。この手法により抗体医薬のみならず,疾患のバイオマーカーや原因タンパク質などを認識するアプタマーを迅速かつ容易に獲得でき,診断薬や治療薬のシーズ創出に繋がっていくことが期待できます。
さらに最近では,抗体医薬原薬の製造現場における簡易定量法の開発(Talana, 277, 126349 (2024))や,次世代バイオ医薬として注目を集めている抗体薬物複合体の定量法や抗体薬物結合比の決定法(Biosens. Bioelectron., 272, 117108 (2025))などを報告しました。
また私達は,いつでも,誰でも,どこでも,簡単に診断できるPoint of Care Testingの開発も進めています。診断が病室や薬局,あるいは自宅で行えれば,より多くの人々の健康管理や治療効果判定,疾患の早期発見に繋がり,薬剤師の職能拡大にも貢献できると考えています。
薬学の分析化学は,自身のアイデアやちょっとした工夫が医療現場や創薬現場で活用されうる実用性も高い学問分野です。あなたのImaginationとCreativityを私達の研究室で発揮してみませんか?
最近の3研からの論文発表
1) Yamada et al., Biosens. Bioelectron., 272, 117108 (2025)
2) Yamada et al., Talana, 277, 126349 (2024)
3) Hirayama and Kuno et al., Chromatography, 44, 45 (2023)
4) Hamada et al., Anal. Sci., 39, 125 (2023)
5) Tong et al., J. Pharm. Biomed. Anal. Open, 1, 100006 (2023)
6) Saito et al., Biosens. Bioelectron., 203, 114027 (2022)
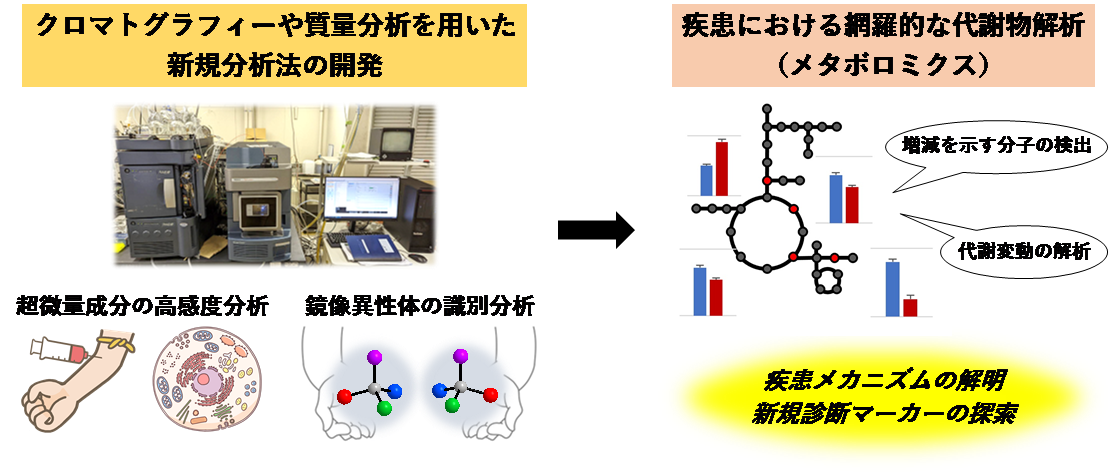
がんや糖尿病などの様々な疾患において、アミノ酸や有機酸といった生体内分子の含量には変化が生じます。生体内の代謝物を網羅的に分析する”メタボロミクス”によって代謝変動を捉えることで、疾患メカニズムの解明や新規診断法の開発に繋がることが期待できます。
生体内に微量にしか存在しない分子や疾患における変動が僅かな分子を測定するためには、高い感度と選択性を兼ね備えた分析法が必要です。我々は液体クロマトグラフィーや質量分析を利用して、アミノ酸をはじめとする低分子化合物のメタボロミクス解析に取り組んでいます。対象物質の誘導体化や分析・検出条件を工夫することで、現在、細胞レベルでの分析を実現しています。
また多くの生体内分子はキラルであり、鏡像異性体間で代謝経路や生理機能が異なるため、これらを識別した分析法の開発にも取り組んでいます。
第1研究室は、等温核酸増幅法の一種である「リコンビナーゼポリメラーゼ増幅(RPA)法」に関する研究を行っています。
このRPA法は、ポリメラーゼ連鎖反応(PCR)法とは異なり、反応液の温度の上げ下げをする必要が無いため、PCRよりも速く核酸(DNA)を増幅できる特長があります。また、RPA法では体温と同程度の37℃付近で反応液を温めるだけで迅速に核酸増幅を行えるため、“特別な装置を必要としない迅速・簡便な核酸増幅検査”への応用に向けた研究が多数行われています。
そのようななか、現在、私たちはRPA法の反応自体の改良に取り組んでいます。RPAの核酸増幅速度のさらなる向上を目指し、使用する新規な酵素を組換え大腸菌などを用いて自家調製したり、アミノ酸残基を置換してより良い酵素に作り変えたりしています。今後は、RPA法による核酸増幅検査の社会実装に向けた研究にも取り組んでいきたいと考えています。
RPAに関する論文発表
1) Kojima et al., J. Biosci. Bioeng., 136, 341 (2023)
2) Kojima et al., J. Biosci. Bioeng., 131, 219 (2021)
