研究内容
生体内において運動機能を担う骨格筋は、多数の長大な筋線維から成り立っています。生体活動に伴う絶え間ない収縮、弛緩により筋線維は常に負荷を受けており、それにともなう物理的なダメージから保護される必要があります。例えば筋細胞膜に存在するタンパク質群は、形質膜の構造安定を担っており、それら構造タンパク質の変異により、骨格筋疾患である筋ジストロフィーが惹起されます。これまで私たちは膜タンパク質ジストログリカンに着目して研究を行ってきました。その過程でジストログリカンの糖鎖修飾が、細胞外マトリックス‐ジストログリカン‐細胞骨格の構造軸を形成する上で重要であること、さらにジストログリカン糖鎖不全が筋疾患発症に直接関与することを明らかにしました(Hara et al., New Engl. J. Med., 2011; Proc. Natl. Acad. Sci. USA., 2011、図1)。
現在、私たちは以下の研究項目を行うことで、神経・筋疾患の発症機構の解明および治療法開発を目指しています。これらの研究は、単に骨格筋組織の再生という観点だけでなく、老齢期の筋委縮や筋力低下をはじめとする高齢化社会の諸問題に対しても、重要な知見をもたらすと期待されます。

(図1:膜タンパク質ジストログリカンの機能破綻による、筋疾患発症機構)
1. 「メカノバイオロジー」を基軸とした筋線維の再生機構に関する研究
絶え間ない筋収縮・弛緩に伴いダメージを受けた筋線維は、筋線維の細胞膜を修復する機構や、新たに筋管を新生する機構を有しており、骨格筋の恒常性が保たれています。特に骨格筋に存在する筋幹細胞(筋衛星細胞)から派生した筋芽細胞は、互いに融合し合うことで筋線維を新生することが知られています。私たちはこれまでに、細胞融合における細胞膜に掛かる物理的な力に着目し、特に細胞外から細胞内にカルシウムイオンを透過するイオンチャネルの一つが膜に掛かる力を感知し活性化されることで、秩序だった筋管の形態形成に関わることを見出しました(Tsuchiya et al., Nat. Commun., 2018; 図2)。さらに、筋衛星細胞に高発現する機械受容イオンチャネル PIEZO1 や TRPM7 が、物理的な刺激を受容してイオン透過を引き起こし、筋幹細胞の活性化や筋再生過程を制御することも明らかにしてきました(Hirano et al., Life Sci. Alliance, 2023, Hirano et al., Science Advances, 2025; 図2)。現在はこれらの知見を発展させ、細胞膜に掛かる力を感知する分子機構がいかに筋再生をもたらすのか、その全体像の解明に取り組んでいます。この研究をさらに発展させ、細胞膜に掛かる力を感知する機構がいかに筋再生をもたらすのか、解明に取り組んでいます。
また、上記研究のもと、力を感知する膜タンパク質群に対し特異的に作用する化合物の探索・開発を通じ、神経・筋疾患に対する治療戦略の構築も目指しています。
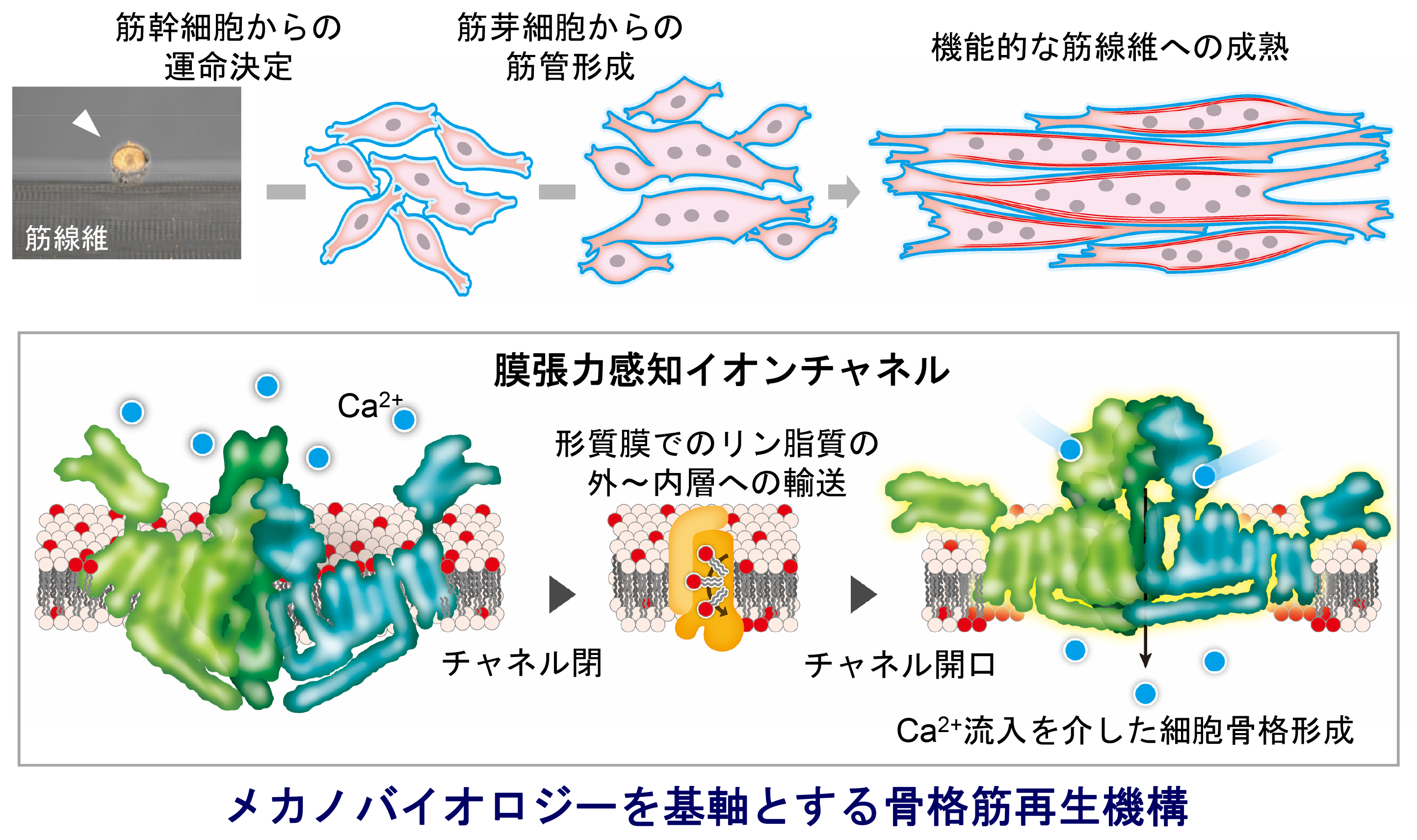
(図2:膜張力を感知するイオンチャネル群による、骨格筋線維の再生機構)
2. 脂質二重層間における脂質輸送機構とその意義に関する研究
生体膜は、生体の基本単位である細胞を形作るもっとも重要な因子ともいえます。生体膜はその基本構造であるリン脂質の性質をもとに、親水性を示す頭部が表面に、疎水性を示すアシル鎖を内側に向けることで、脂質二重層という安定な構造をとります。極性基の種類や脂肪酸の鎖長・不飽和度の違いにより、非常に数多くの分子種が生体内に存在します。興味深いことに、哺乳動物の細胞では、生体膜の外側と内側を構成する脂質分子が異なっており、この「脂質分子の非対称分布」が生体膜の構造や膜物性の変化、細胞内情報伝達など、細胞・生体機能に重要な役割を果たすことが明らかになりつつあります。私たちは、脂質二重層におけるリン脂質の非対称分布をもたらす「リン脂質フリップ・フロップ(とんぼ返り運動)」が、いかに膜タンパク質の作用に影響を及ぼすのか、特にイオンチャネルへの活性制御という観点から解明を目指しています(図3)。
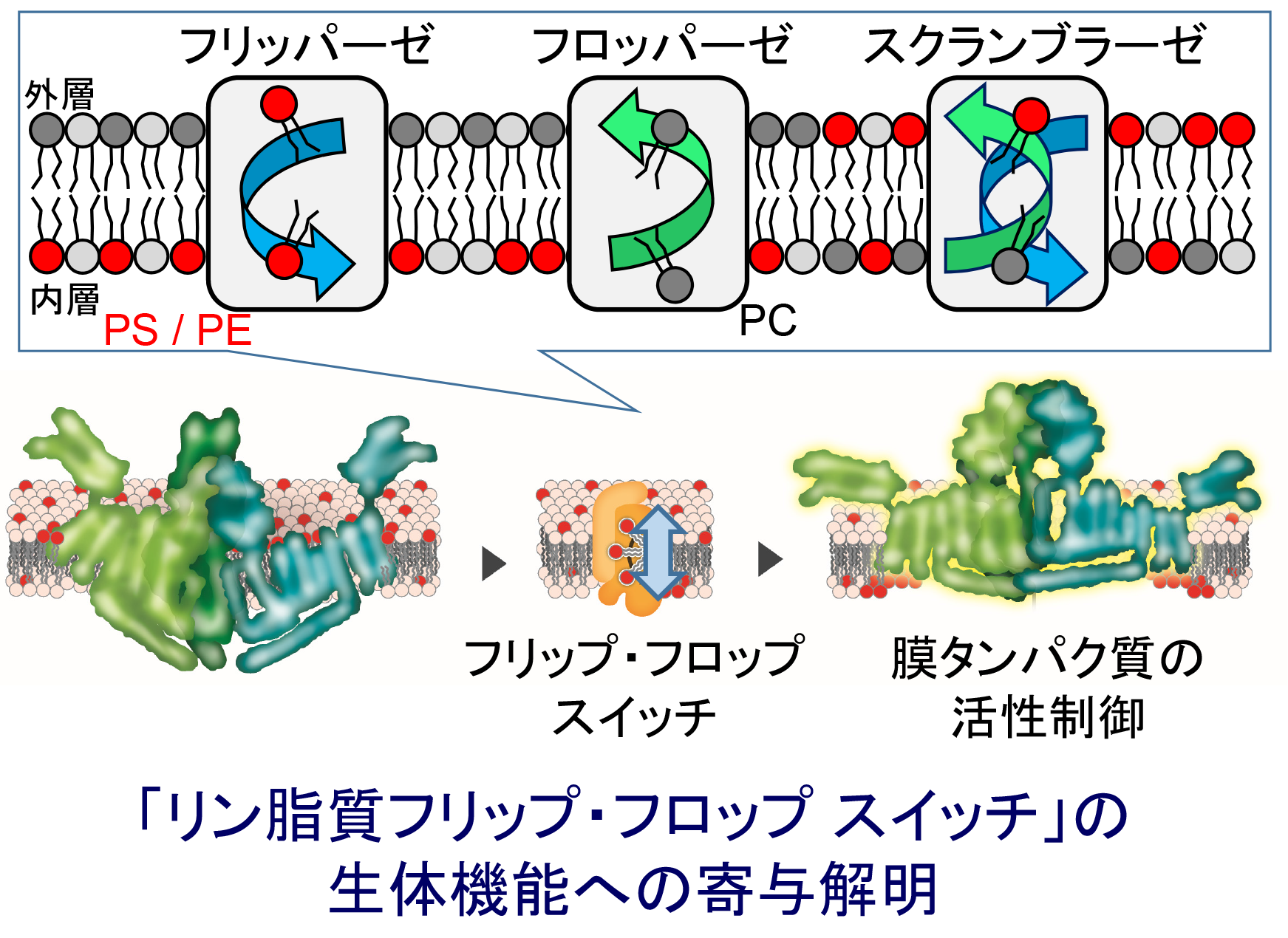
(図3:生体膜における脂質分子の非対称分布による、膜タンパク質制御機構)
3. 亜鉛シグナリングを介した脳神経機能調節に関する研究
脳神経系は直接あるいは内分泌系を介して生体の働きを制御する司令塔の役割を担っています。そこで、必須微量金属である亜鉛から視た脳の機能解析と病態解析を行っています。亜鉛イオンはグルタミン酸作動性神経終末において細胞内外でシグナルファクターとして記憶の獲得・維持・想起に関与します。シナプス亜鉛イオンの恒常性は、厳密に制御されているため、その破綻により認知活動が障害されます。これまでに、アルツハイマー病の原因物質とされるアミロイドβによる認知活動の障害、ストレスによる神経内分泌機能の乱れによる認知活動の障害、さらにはパーキンソン病発症の要因とされる黒質ドパミン作動性神経変性に対して、細胞内亜鉛イオンの恒常性破綻が関与することを明らかにしつつあります。従来から着目されているカルシウムシグナリングのみならず、亜鉛シグナリングの異常が認知機能障害や神経変性疾患の要因となるのではないか、という観点から、本研究を発展させ、脳神経機能調節機構や病態の解明を目指しています。

(図4:神経細胞内亜鉛イオン恒常性破綻による神経機能の障害)
